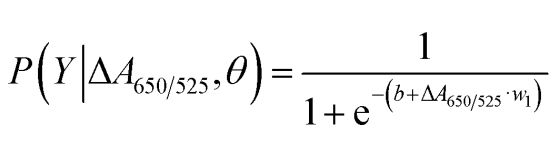Vēža agrīna atklāšana, izmantojot šķidro biopsiju, ir jauns vēža atklāšanas un diagnostikas virziens, ko pēdējos gados ierosinājis ASV Nacionālais vēža institūts, kura mērķis ir atklāt agrīnu vēzi vai pat pirmsvēža bojājumus. Tā ir plaši izmantota kā jauns biomarķieris dažādu ļaundabīgu audzēju, tostarp plaušu vēža, kuņģa-zarnu trakta audzēju, gliomu un ginekoloģisko audzēju, agrīnai diagnostikai.
Metilācijas ainavas (Methylscape) biomarķieru identificēšanas platformu parādīšanās varētu ievērojami uzlabot esošo agrīno vēža skrīningu, nodrošinot pacientiem agrīnāko ārstējamo stadiju.
Nesen pētnieki ir izstrādājuši vienkāršu un tiešas uztveršanas platformu metilēšanas ainavas noteikšanai, kuras pamatā ir ar cisteamīnu dekorētas zelta nanodaļiņas (Cist/AuNP) apvienojumā ar viedtālruņa biosensoru, kas ļauj ātri un agrīni veikt plaša spektra audzēju skrīningu. Agrīnu leikēmijas skrīningu var veikt 15 minūšu laikā pēc DNS ekstrakcijas no asins parauga ar 90,0% precizitāti. Raksta nosaukums ir "Ātra vēža DNS noteikšana cilvēka asinīs, izmantojot ar cisteamīnu dekorētas AuNP un mašīnmācīšanās iespējotu viedtālruni".
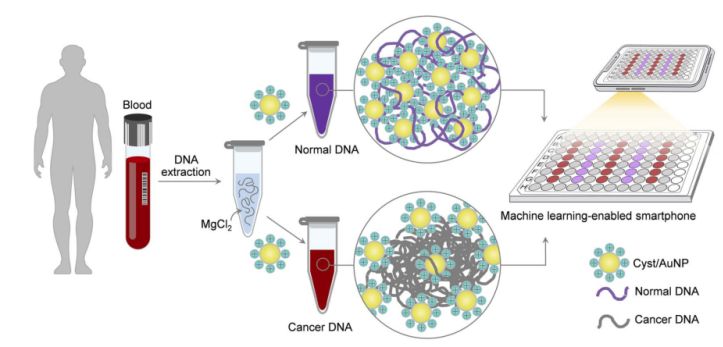
1. attēls. Vienkārša un ātra uztveršanas platforma vēža skrīningam, izmantojot cistas/AuNP komponentus, var tikt izveidota divos vienkāršos soļos.
Tas ir parādīts 1. attēlā. Vispirms DNS fragmentu izšķīdināšanai tika izmantots ūdens šķīdums. Pēc tam sajauktajam šķīdumam tika pievienotas cistas/AuNP. Normālai un ļaundabīgai DNS ir atšķirīgas metilēšanas īpašības, kā rezultātā DNS fragmentiem ir atšķirīgi pašsalikšanās modeļi. Normāla DNS brīvi agregējas un galu galā agregē cistas/AuNP, kā rezultātā cistas/AuNP ir sarkanās krāsas nobīdes raksturs, tāpēc krāsas maiņu no sarkanas uz violetu var novērot ar neapbruņotu aci. Turpretī vēža DNS unikālais metilēšanas profils noved pie lielāku DNS fragmentu kopu veidošanās.
96 iedobju plākšņu attēli tika uzņemti, izmantojot viedtālruņa kameru. Vēža DNS tika mērīta ar viedtālruni, kas aprīkots ar mašīnmācīšanos, salīdzinot ar spektroskopijas metodēm.
Vēža skrīnings reālos asins paraugos
Lai paplašinātu uztveršanas platformas lietderību, pētnieki izmantoja sensoru, kas veiksmīgi atšķīra normālu un vēža DNS reālos asins paraugos. Metilēšanas modeļi CpG vietās epigenetiski regulē gēnu ekspresiju. Gandrīz visos vēža veidos ir novērotas izmaiņas DNS metilēšanā un līdz ar to arī gēnu ekspresijā, kas veicina audzēja veidošanos.
Kā modeli citiem ar DNS metilēšanu saistītiem vēža veidiem pētnieki izmantoja leikēmijas pacientu un veselīgu kontroles grupu asins paraugus, lai izpētītu metilēšanas ainavas efektivitāti leikēmisko vēža veidu diferenciācijā. Šis metilēšanas ainavas biomarķieris ne tikai pārspēj esošās ātrās leikēmijas skrīninga metodes, bet arī pierāda, ka, izmantojot šo vienkāršo un tiešo testu, ir iespējams atklāt plašu vēža veidu klāstu agrīnā stadijā.
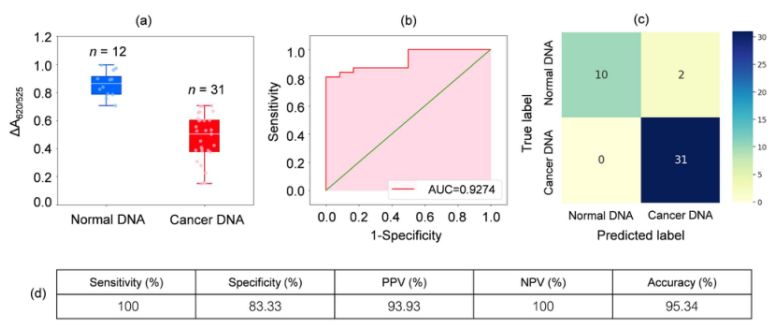
Tika analizēta DNS no 31 leikēmijas pacienta un 12 veselu indivīdu asins paraugiem. Kā parādīts 2.a attēla lodziņu diagrammā, vēža paraugu relatīvā absorbcija (ΔA650/525) bija zemāka nekā normālu paraugu DNS. Tas galvenokārt bija saistīts ar paaugstinātu hidrofobitāti, kas noveda pie blīvas vēža DNS agregācijas, kas novērsa cistas/AuNP agregāciju. Rezultātā šīs nanodaļiņas bija pilnībā izkliedētas vēža agregātu ārējos slāņos, kā rezultātā cistas/AuNP, kas adsorbētas uz normāliem un vēža DNS agregātiem, izkliede bija atšķirīga. Pēc tam ROC līknes tika ģenerētas, mainot slieksni no minimālās vērtības ΔA650/525 līdz maksimālajai vērtībai.
2. attēls. (a) Cistu/AuNP šķīdumu relatīvās absorbcijas vērtības, kas parāda normālas (zilā) un vēža (sarkanā) DNS klātbūtni optimizētos apstākļos.
(DA650/525) lodziņu diagrammas; (b) ROC analīze un diagnostisko testu novērtējums. (c) Sajaukšanas matrica normālu un vēža pacientu diagnostikai. (d) Izstrādātās metodes jutīgums, specifiskums, pozitīvā paredzamā vērtība (PPV), negatīvā paredzamā vērtība (NPV) un precizitāte.
Kā parādīts 2.b attēlā, izstrādātajam sensoram iegūtais laukums zem ROC līknes (AUC = 0,9274) uzrādīja augstu jutību un specifiskumu. Kā redzams no lodziņu diagrammas, zemākais punkts, kas attēlo normālu DNS grupu, nav labi atdalīts no augstākā punkta, kas attēlo vēža DNS grupu; tāpēc, lai atšķirtu normālu un vēža grupas, tika izmantota loģistiskā regresija. Ņemot vērā neatkarīgu mainīgo kopu, tas novērtē notikuma, piemēram, vēža vai normālas grupas, iestāšanās varbūtību. Atkarīgais mainīgais svārstās no 0 līdz 1. Tāpēc rezultāts ir varbūtība. Mēs noteicām vēža identificēšanas varbūtību (P), pamatojoties uz ΔA650/525, šādi.
kur b=5,3533, w1=-6,965. Parauga klasifikācijai varbūtība, kas mazāka par 0,5, norāda uz normālu paraugu, savukārt varbūtība, kas ir 0,5 vai lielāka, norāda uz vēža paraugu. 2.c attēlā redzama apjukuma matrica, kas ģenerēta no nemainītas krustvalidācijas, kas tika izmantota, lai validētu klasifikācijas metodes stabilitāti. 2.d attēlā ir apkopots metodes diagnostisko testu novērtējums, tostarp jutīgums, specifiskums, pozitīvā paredzamā vērtība (PPV) un negatīvā paredzamā vērtība (NPV).
Viedtālruņos balstīti biosensori
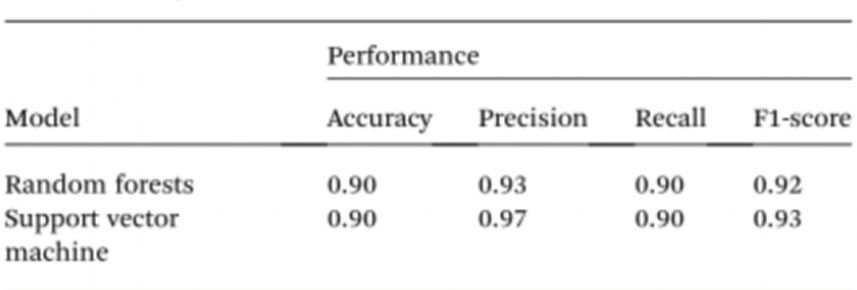
Lai vēl vairāk vienkāršotu paraugu testēšanu, neizmantojot spektrofotometrus, pētnieki izmantoja mākslīgo intelektu (MI), lai interpretētu šķīduma krāsu un atšķirtu normālus un vēža slimniekus. Ņemot to vērā, datorredze tika izmantota, lai, izmantojot 96 iedobju plākšņu attēlus, kas uzņemti ar mobilā tālruņa kameru, pārvērstu cistu/AuNP šķīduma krāsu normālā DNS (violetā) vai vēža DNS (sarkanā) krāsā. Mākslīgais intelekts var samazināt izmaksas un uzlabot nanodaļiņu šķīdumu krāsas interpretācijas pieejamību, neizmantojot nekādus optiskos viedtālruņu piederumus. Visbeidzot, modeļu konstruēšanai tika apmācīti divi mašīnmācīšanās modeļi, tostarp Random Forest (RF) un Support Vector Machine (SVM). Gan RF, gan SVM modeļi pareizi klasificēja paraugus kā pozitīvus un negatīvus ar 90,0% precizitāti. Tas liecina, ka mākslīgā intelekta izmantošana mobilo tālruņu biosensoros ir pilnīgi iespējama.
3. attēls. (a) Šķīduma mērķa klase, kas reģistrēta parauga sagatavošanas laikā attēla iegūšanas posmam. (b) Attēla piemērs, kas uzņemts attēla iegūšanas posmā. (c) Cistu/AuNP šķīduma krāsas intensitāte katrā 96 iedobju plāksnes iedobē, kas iegūta no attēla (b).
Izmantojot cistas/AuNP, pētnieki ir veiksmīgi izstrādājuši vienkāršu uztveršanas platformu metilēšanas ainavas noteikšanai un sensoru, kas spēj atšķirt normālu DNS no vēža DNS, leikēmijas skrīningam izmantojot reālus asins paraugus. Izstrādātais sensors pierādīja, ka no reāliem asins paraugiem iegūta DNS spēja ātri un rentabli noteikt nelielu daudzumu vēža DNS (3nM) leikēmijas pacientiem 15 minūtēs un uzrādīja 95,3% precizitāti. Lai vēl vairāk vienkāršotu paraugu testēšanu, novēršot nepieciešamību pēc spektrofotometra, tika izmantota mašīnmācīšanās, lai interpretētu šķīduma krāsu un atšķirtu normālus un vēža slimniekus, izmantojot mobilā tālruņa fotogrāfiju, un arī precizitāte tika sasniegta 90,0% apmērā.
Atsauce: DOI: 10.1039/d2ra05725e
Publicēšanas laiks: 2023. gada 18. februāris
 中文网站
中文网站